Konferencia otvorila diskusiu: HTA metodika má byť základom spravodlivého financovania zdravotníctva
Minulý mesiac sa na pôde ministerstva zdravotníctva konala HTA konferencia, ktorú zorganizovalo slovenské NIHO.

Časový horizont, v akom sa môže legislatíva a usmernenia meniť, nezávisí od toho, či je to krátko alebo dlho od zmeny predchádzajúceho aktu riadenia, ale od toho či sa skutoční experti zhodujú na tom, či systém funguje alebo nefunguje efektívne.
Predovšetkým je potrebné zdôrazniť, že návrh Metodického usmernenia pre hodnotenie zdravotníckych technológií (ďalej len „HTA“), ktorý bol predstavený na konferencii HTA methodological guideline for Slovakia konanej 30. septembra 2025 na Ministerstve zdravotníctva SR, nie je novým, záväzným metodickým usmernením – ide o návrh medzinárodne uznávaných expertov v oblasti HTA, ktorí na základe svojich rozsiahlych skúseností s prípravou obdobných usmernení pre iné štáty odporúčajú, čo by malo metodické usmernenie v Slovenskej republike obsahovať pre optimálne vykonávanie HTA.
{{odporucane}}
Akékoľvek metodické usmernenie musí byť v súlade s platnou legislatívou – zákonom č. 363/2011 Z. z. a vyhláškou Ministerstva zdravotníctva SR o farmako-ekonomickom rozbore lieku (ďalej len „vyhláška o FER“), ktorá sa vydáva na základe zákona. Vyhláška o FER v aktuálnom znení ustanovuje konkrétne náležitosti FER predkladaného držiteľom registrácie lieku. Návrh usmernenia odprezentovaný na konferencii odporúča zásadne iné náležitosti FER ako platná vyhláška o FER.
Prehľad najdôležitejších (z hľadiska legislatívy) rozdielov:
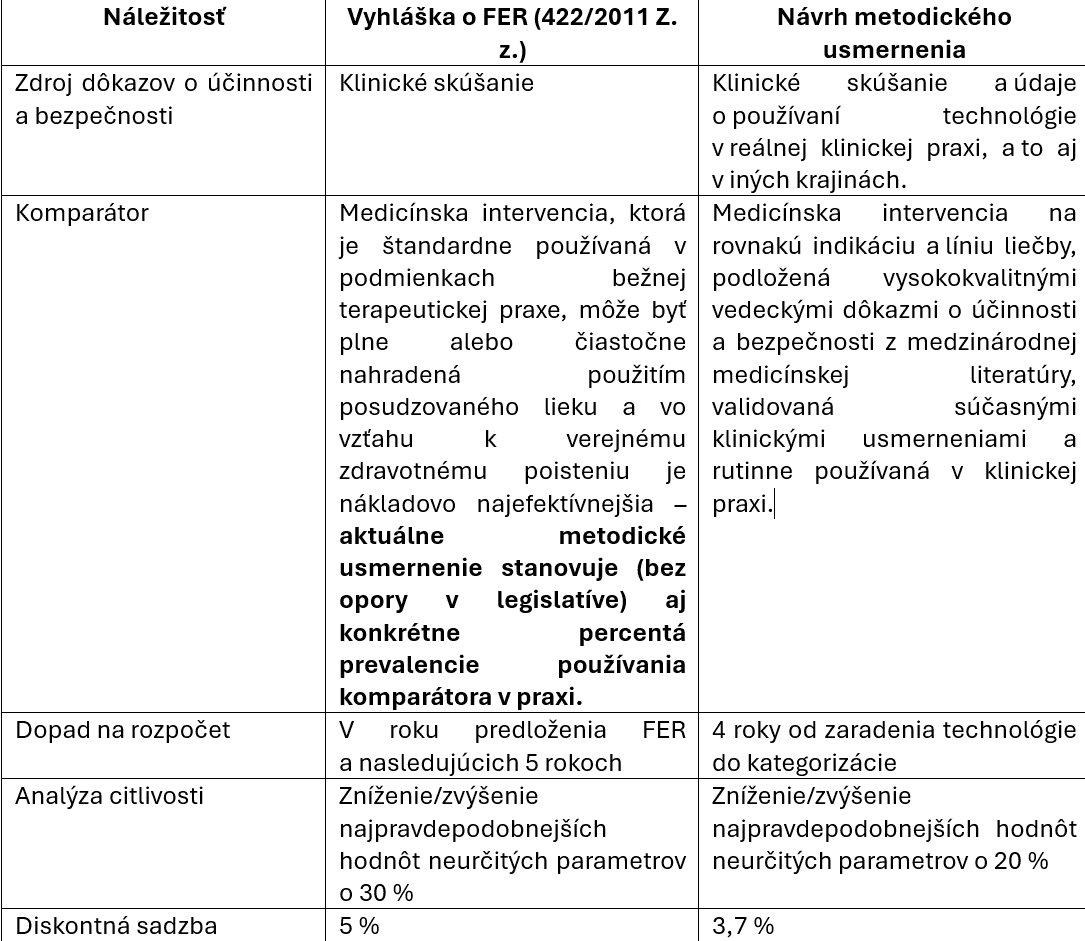
Už z tohto prehľadu rozdielov je zrejmé, že nové metodické usmernenie nie je možné implementovať bez zmeny legislatívy.
Uvedený prehľad rozdielov sa týka iba konkrétnych rozdielov medzi vyhláškou o FER a návrhom nového metodického usmernenia. Medzinárodní experti zároveň identifikovali aj viacero zásadných nedostatkov v súčasnosti platného metodického usmernenia, a to najmä:
- platné usmernenie zmiešava metodiku HTA s procesnými otázkami (napr. „začierňovanie“ dôverných informácií) nekomplexným a nezrozumiteľným spôsobom,
- zbytočne diskutuje rôzne dilemy (napr. vhodná diskontná sadzba pre SR) – metodika má byť jednoznačná,
- nadmerná pozornosť sa venuje praxi v iných štátoch (najmä ČR a Anglicko) – metodika pre SR má riešiť SR,
- viaceré koncepty sú popisované príliš (napr. najvhodnejšia metóda pre korekciu cyklu v modeli), iným nie je venovaná dostatočná pozornosť (záťaž ochorenia, nenaplnená medicínska potreba),
- metodika obsahuje poučky zo starších učebníc (napr. pri vysvetľovaní QALY), - v metodike sú zaradené aj obsolentné informácie (napr. EBM pyramída) – údaje z reálnej praxe sú v súčasnosti považované za rovnocenné randomizovaným klinickým skúšaniam,
- viaceré odporúčania sú nezmyselne konkrétne (napr. odporúčaná rýchlosť modelu), iné nedostatočne dopracované a nepoužiteľné naprieč terapeutickými oblasťami (napr. odporúčaná tabuľka vyvinutá iba pre ochorenia so stavmi bez progresie a po progresii).
Preto nie je možné aktualizovať platné usmernenie, ale je potrebné pristúpiť k príprave nového metodického usmernenia.
Autori návrhu tiež odporúčajú, aby sa nové usmernenie uplatňovalo nielen na lieky, ale aj na zdravotnícke pomôcky a ďalšie technológie. V záujme udržateľnosti financovania zdravotnej starostlivosti a elementárnej spravodlivosti je nanajvýš žiadúce analyzovať hodnotu všetkých zdravotníckych technológií pre konkrétny zdravotnícky systém na základe rovnakých kritérií (s možnými odchýlkami v prípade legislatívou definovaného osobitného charakteru technológie).
{{suvisiace}}
Z pohľadu NIHO by bolo vhodné pripraviť návrh novej vyhlášky o FER, ktorej prílohou by bolo metodické usmernenie v navrhovanom znení. Návrh vyhlášky (spolu s návrhom usmernenia) by sa následne predložil do legislatívneho procesu. V rámci medzirezortného pripomienkového konania by tak mohli všetci stakeholderi (farmaceutický priemysel, zdravotné poisťovne, pacientske organizácie, odborné spoločnosti) a ďalší zástupcovia odbornej a laickej verejnosti uplatniť svoje pripomienky a návrhy na zlepšenie predloženého materiálu. Zároveň je možné uvažovať aj o tom, aby sa nové usmernenie vzťahovalo aj na hodnotenie zdravotníckych pomôcok – v takom prípade by bolo nutné pripraviť aj novú vyhlášku o ich medicínsko-ekonomickom rozbore.
Konferenciu, na ktorej bol návrh predstavený, vnímame ako prvý krok k otvoreniu diskusie o aktualizácií postupov súvisiacich s vykonávaním HTA v podmienkach Slovenskej republiky. S týmto cieľom Národný inštitút pre hodnotu a technológie v zdravotníctve spolu s Katedrou organizácie a riadenia farmácie Farmaceutickej fakulty UK uvedenú konferenciu organizovali. Ako vo svojom príhovore na konferencii zdôraznil pán minister Šaško – nová metodika HTA má byť súčasťou celého “balíka“ legislatívnych zmien, zahŕňajúceho rozsiahlu novelu zákona č. 363/2011 Z. z. a nových vykonávacích predpisov k zákonu.
Článok vyšiel pôvodne v Zdravotníckych novinách.
Celý obsah článku je prístupný pre predplatiteľov
Celý obsah článku je prístupný pre predplatiteľov
Momentálne nemáte aktívne žiadne predplatné.








.jpg)
.jpg)
